
胃癌是发病率极高的恶性肿瘤之一,其死亡率也仅仅低于肺癌和肝癌,它的预后较差,严重危害人民健康,是肿瘤防治研究中的重点。胃癌治疗方法主要包括手术治疗、化疗,放疗、免疫治疗以及分子靶向治疗,其中,化疗是非常重要的治疗手段,但在临床实践中,化疗耐药性限制了各药物的临床疗效。
有研究表明,胃癌可能对铁死亡(ferroptosis,一种细胞死亡的形式,由脂质过氧化物的铁依赖性积累引起,铁死亡特征包括脂质过氧化和铁代谢)敏感,但是介导铁死亡的信号通路并不明确,基于此,Shumin Ouyang团队研究了铁死亡和胃癌生长的相关性,并于2022年6月于Redox Biol杂志上发表了题为Inhibition of STAT3-ferroptosis negative regulatory axis suppresses tumor growth and alleviates chemoresistance in gastric cancer的研究,发现STAT3(信号转导和转录激活因子3,具有信号转导和转录激活双重功能的关键致癌基因)是铁死亡的负调控因子,并且且诱导铁死亡可显著抑制肿瘤的生长、减轻化疗耐药性。

研究之初,作者探索了TCGA和GTEx数据库,推测铁死亡负调控与胃癌生长和胃癌患者的低生存率显著相关,为了验证这一点,团队建立了对5-氟尿嘧啶有耐药性的人胃癌细胞系,用正常人胃癌细胞系作对照,进行cDNA微阵列分析发现具有耐药性的胃癌细胞系中铁死亡负调控信号的关键基因显著上调。鉴于肿瘤类器官与临床肿瘤对治疗药物的反应非常相似,于是团队建立了三个人胃癌类器官群体,一个使用爱拉斯汀进行诱导铁死亡处理,第二个使用5-氟尿嘧啶进行建立耐药性实验,然后第三组使用二者共同处理,作者把三组结果进行对比,发现有耐药性的胃癌类器官,在诱导发生铁死亡后其对5-氟尿嘧啶的敏感性极大的增强。这些结果表明铁死亡负调控与胃癌的生长和5-氟尿嘧啶耐药密切相关。(图1)
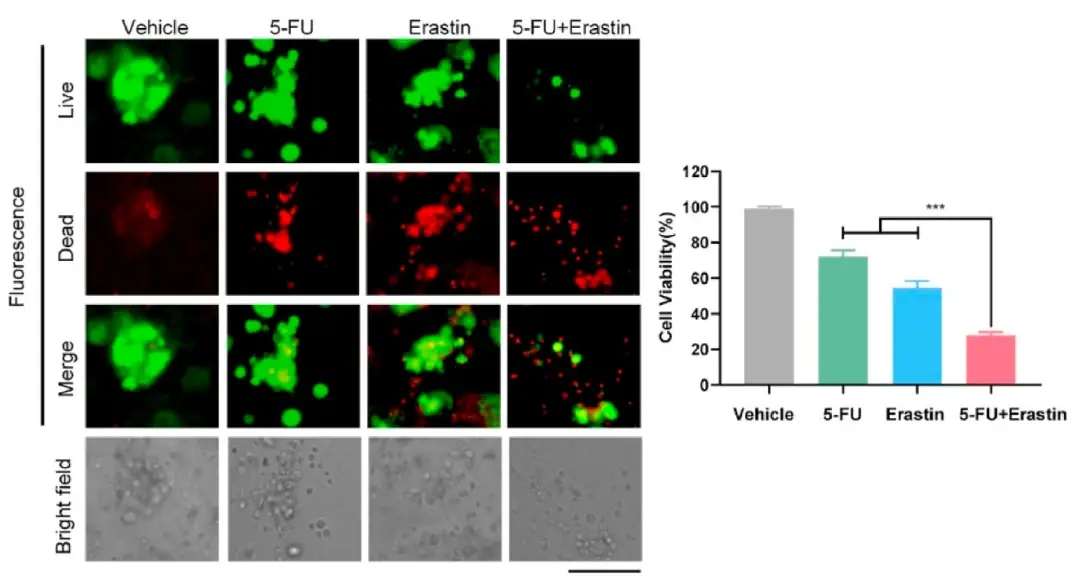
图1 铁死亡负调控(FNR)信号和胃癌生长和化疗耐药有关
作者考虑到STAT3基因在胃癌中高表达,为了研究STAT3与铁死亡之间的关系,作者敲除了人胃癌细胞系的STAT3并进行了转录组分析。基因富集分析结果显示铁死亡负调控信号是由STAT3敲除介导的,且在进行了RT-PCR分析后发现敲除STAT3在mRNA和蛋白水平上均显著抑制了铁死亡抑制因子的表达。然后,团队利用透射电镜检测了敲除STAT3的胃癌细胞的形态学变化,发现敲除STAT3的胃癌细胞出现了线粒体萎缩、膜密度增加的特征,随后对胞内脂质过氧化和铁含量水平进行检测,发现STAT3基因下调导致脂质过氧化水平和胞内铁含量升高。这些结果与铁死亡的特征相符合,表明抑制STAT3可引发胃癌细胞发生铁死亡。(图2)
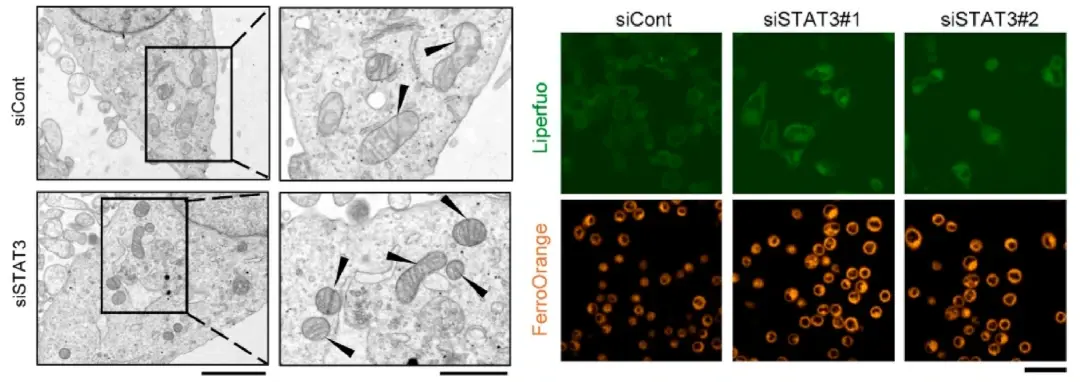
图2 抑制STAT3可触发铁死亡中的铁依赖性氧化损伤,并抑制胃癌细胞的增殖和存活
根据上述结果,作者推测,STAT3可能是铁死亡的负调控因子,其抑制剂可能作为一种有效的抗癌药物。本文选择W1131(STAT3抑制剂)进行进一步研究,首先作者在无胸腺裸鼠中建立了胃癌PDX模型,并对PDX衍生的类器官采用四种药物方案处理(对照组\铁死亡抑制剂\STAT3抑制剂\STAT3抑制剂+铁死亡抑制剂),发现W1131确实抑制了胃癌类器官的生长,在此基础上使用铁死亡抑制剂处理,进一步发现W1131引起的抑制效果可以通过铁死亡抑制剂的处理大幅度减弱。此外,团队检测了类器官中脂质过氧化产物的含量,发现W1131的处理能显著增加脂质过氧化产物蛋白加合物的含量。这些结果表明,W1131可作为一种有效的抗癌药物,通过抑制STAT3信号通路和诱导铁死亡显著抑制肿瘤的生长。(图3)
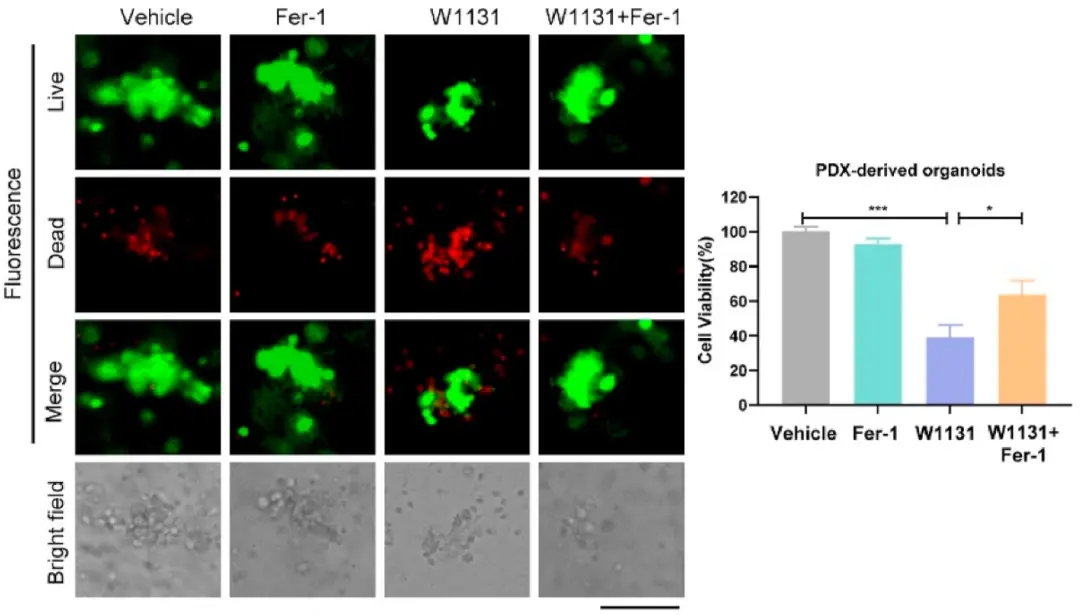
图3 PDX衍生的类器官四种药物方案处理
最后,作者研究了STAT3抑制剂W1131和胃癌耐药性之间的关系。作者建立了胃癌类器官模型,设计了四组用药方案(正常培养\5-氟尿嘧啶\W1131\5-氟尿嘧啶+W1131),经过培养后进行细胞活力测定,结果表明W1131与5-氟尿嘧啶共同处理的类器官细胞活性明显低于5-氟尿嘧啶单独处理的,说明W1131显著提高了胃癌类器官对药物5-氟尿嘧啶的敏感性,且从类器官克隆数统计分析也能得到相同的结果。总之,STAT3抑制剂W1131能够明显缓解胃癌的化疗耐药性。
总的来说,本文作者借助胃癌类器官模型,验证了胃癌对铁死亡敏感的现象并进一步得出结论:STAT3是铁死亡的负调控因子,抑制STAT3可引发铁死亡进而抑制胃癌的生长、减轻化疗耐药性。这一结论的发现,为胃癌治疗和解决化疗耐药问题提供了一个新的思路:可以进一步探究STAT3相关的抑制剂在肿瘤发生中的重要作用,同时这也为新药研发提供了潜在的治疗靶点。
